En ny preprintstudie tyder på att gravida får samma antikroppsnivåer som icke-gravida kvinnor när de vaccineras med mRNA-vaccinen mot COVID-19. Denna och ytterligare data tyder även på att gravida kvinnors biverkningsfrekvens också är jämförbar. Antikroppssvaret hos vaccinerade gravida kvinnor tycks därtill överstiga det hos gravida kvinnor som i stället tidigare har haft COVID-19.
- Gray et al. vid Harvard studerade 131 kvinnor i reproduktiv ålder (de hade urvalet 18-45 år), varav 84 var gravida, 31 ammade, 16 var icke-gravida. De flesta var i 30-årsåldern. De flesta som fick sin första vaccindos var i 2:a (46%) eller 3:e (40%) trimestern. De gravida var i snitt i vecka 23.2
- I studien tittade forskarna på vaccinering med Pfizers och Modernas vaccin (de som var godkända vid tidpunkten i USA). Blodprover togs vid baseline, vid dos 2, samt 2-5.5 veckor efter dos 2. Därtill togs prover vid födseln om det inträffade unders studieperioden (13 individer)
- De jämförde antikroppsnivåerna med 37 kvinnor som 4-12 veckor innan provtagningen haft COVID-19. Som ses i den övre delen av figuren nedanför (panelen längst ner till höger) så var IgG-antikroppsnivåerna efter vaccination signifikant högre jämfört med nivåerna efter tidigare infektion.
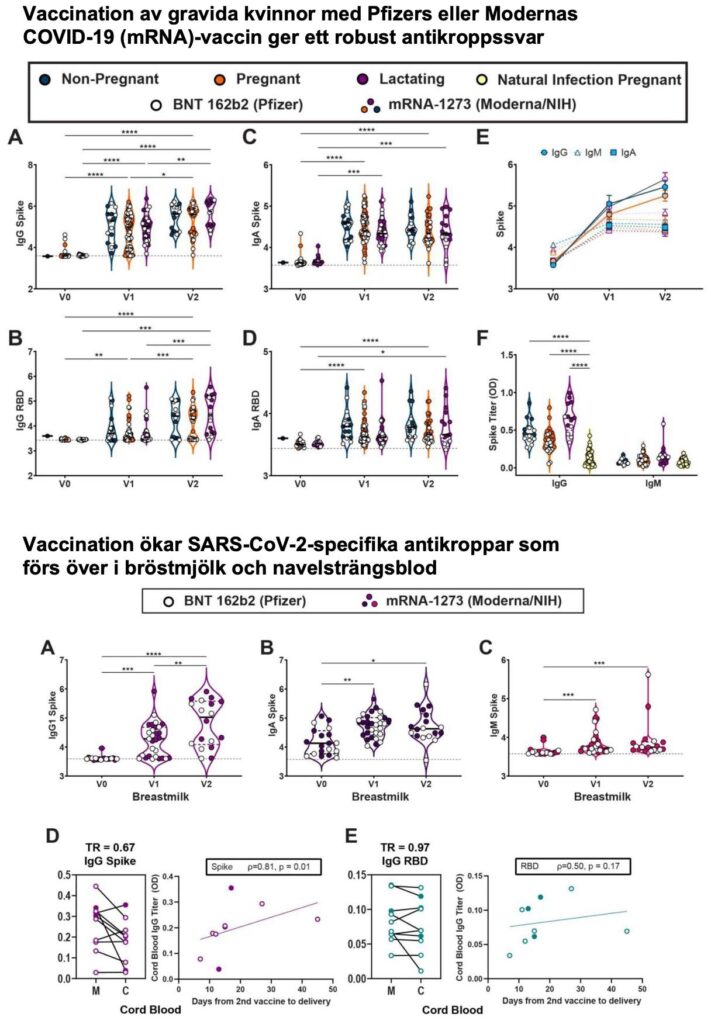
Antikroppar i navelsträngsblod och bröstmjölken efter vaccinering
- I navelsträngsblod (10 av 10 prover) och i bröstmjölken fanns antikroppar av ffa. typen IgG. En andra dos ökade nivåerna av IgG i moderns blod och bröstmjölken. Sådan överföring av antikroppar har tidigare observerats för de antikroppar som uppstår efter infektion med SARS-CoV-2 (studie här i JAMA Pediatrics). Man har tidigare spekulerat i huruvida sådana antikroppar kan skydda fostret från infektion med SARS-CoV-2 (så kallad passiv immunisering, mer om det här).
- Signifikant högre antikroppsnivåer sågs med Modernas kontra Pfizers vaccin (se bilden nedanför), något som författarna spekulerar kan ha att göra med det längre dosintervallet (men mRNA-dosen är ju högre för Modernas vaccin; 100 µg kontra 30 µg).
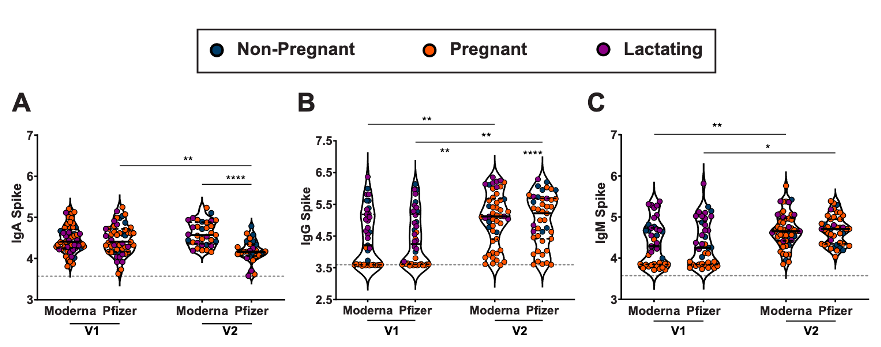
Inte fler biverkningar bland gravida, men generellt sett kanske fler hos kvinnor för mRNA-vaccin
Biverkningarna var – som tidigare observerat med mRNA-vaccinen – vanligare efter dos 2 (se gärna denna sammanställning). T.ex. sågs feber hos 1-6% vid första dosen, för att uppträda hos 32-50% efter den andra dosen. Därtill redovisas intressanta resultat i supplementära tabell nummer 2, där de fann en korrelation med högre nivåer av antikroppar efter vaccinering, och en total symptompoäng – dvs. fler biverkningar tycktes i detta fall korrelera med hur mycket antikroppar kvinnorna senare fick tack vare vaccinen.
De anger även i diskussionen att de i större dataset i USA inte har sett någon data för att vaccinen skulle ge mer biverkningar eller skadliga inverkningar på gravida (ålder 16-54). Detta har de kunnat följa med en smartphone app “V-safe” (se t.ex. här och här på CDC:s hemsida).
V-safe har även använts för att finna att kvinnor generellt sett har rapporterat betydligt fler biverkningar mot COVID-19-vaccinen, jämfört med män (CDC-publikation här).
-
Biverkningsrapporterna Dec 14-Jan 13 avsåg till 79% av fallen kvinnor, för ~7,000 biverkningar rapporterade för de första 13.8 miljoner givna doserna – under denna period utgjorde kvinnor 60% av de som fått vaccin i USA.
-
Tidigare data tyder på könsskillnader i hur effektiva vissa vaccin är (som regel till fördel för kvinnor). Lite relaterat om det i denna långa Twitter-tråd relaterad till könsskillnader vad gäller COVID-19, men som också går igenom lite möjliga mekanismer för könsskillnader i immunförsvaret.
- Att kvinnor rapporterar fler biverkningar kan också bero på att de helt enkelt är bättre och mer villiga att bidra med rapportering, men det finns alltså även immunologiska skillnader som kan tala för varför kvinnor skulle kunna uppleva fler biverkningar – och även bättre skydd – av vaccin.
För den nya preprintsstudien av Gray et al. anger de i diskussionen, baserat på tidigare vaccinkunskap, att man antagligen får olika mängd IgG överfört till fostret beroende på trimester (se t.ex. denna av Palmeira et al.). Denna kinetik är inte känd för COVID-19. De lyfter även att graviditet ökar risken för svår sjukdom, men att man samtidigt inte vet huruvida t.ex. mRNA-vaccin kan påverka fostret – även om ingen data tyder på sådana effekter.
Se gärna även min tidigare sammanställning här om gravida kvinnors och fostrets risk vid COVID-19, och vad WHO/CDC säger om vaccinering
Med vänliga hälsningar,
Jonathan Cedernaes
Leg. läkare, PhD/senior forskare