I Sverige och EU har bivalenta boosterdoser mot COVID-19 börjat rullas ut. Dessa immuniserar dels mot den första Omicron-varianten BA.1, eller BA.4/5, dels mot ursprungsvarianten av SARS-CoV-2 (från 2019/2020). I USA satsade man direkt på vaccinen som inriktar sig på de för tillfället mest dominanta varianterna (BA.4/5), medan man i EU först har godkänt de som inriktar sig på den tidigare Omicron-varianten, BA.1. Klinisk skyddsdata saknas egentligen för bägge vaccinversioner, men antikroppsdata och säkerhetsdata finns från hundratals individer, bl.a. nyligen publicerat av Chalkias et al. i tidskriften New England Journal of Medicine (NEJM).
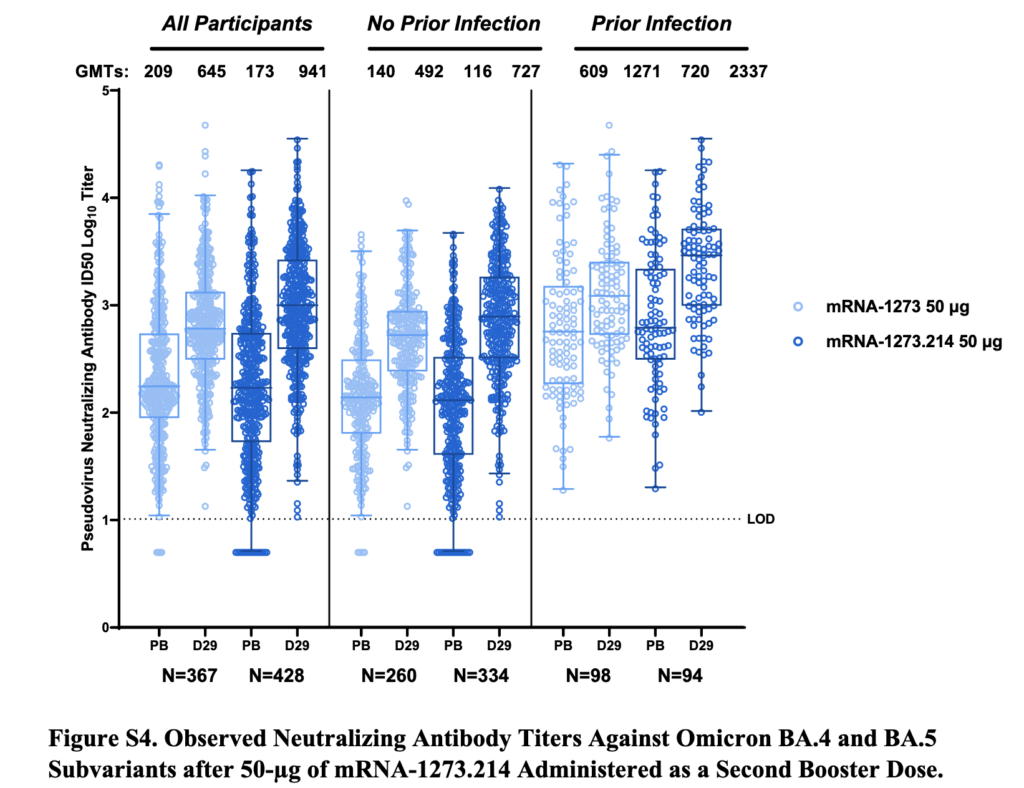
Den nya datan tyder på att vaccinen som nu delvis riktas mot BA.1 – givet som en 4:e dos – också ökar skyddet mot de senare Omicron-subvarianterna (BA.4/5, se skärmdumpen längst ner). Skyddet tycks även öka mer mot de tidigare varianterna, dvs. alpha, beta, gamma och delta – om man tar det uppdaterade boostervaccinet, jämfört med mRNA-vaccin som riktar sig mot den ursprungliga SARS-CoV-2-varianten (“ancestral WH-1”).
Dessa data är ännu i form av labbaserde analyser, som vi dock vet korrelerar mycket väl med det faktiska skyddet (se t.ex. punkt 6 i mitt tidigare blogginlägg här). Datan stämmer även överens med de preliminära data man har sett i studier på möss, där bivalenta vaccindoser ger breddat skydd, inklusive när de ges som första vaccindos (dvs. till tidigare ovaccinerade möss).
Utifrån de mycket snarlika tidigare vaccinversionerna, är säkerhetsdatan för dessa typer av vaccin nu mycket omfattande (även bivalenta vaccin har studerats sen tidigare i viss mån, se t.ex. mitt tidigare inlägg från maj 2021, liksom min genomgång av omfattande säkerhetsdata här). De nyare datan i bl.a. NEJM, tyder också på att säkerhetsprofilen är oförändrad för de nyare, bivalenta vaccinen. NEJM-datan avser Modernas vaccin, men även Pfizer har liknande data, som de har redovisat för CDC.
Vad gäller säkerhetsdatat för boosterdoser, finns därtill ytterligare data som visar att den ovanliga men allvarligare biverkningen myokardit, tycks ses än mer sällan med booster-doser – och det även hos barn (se även studien av Mevorach et al., samt preprintstudien av Vu et al.). Av betydelse är att myokarditrisken tycks minska med ett längre intervall mellan doserna (se t.ex. studien av Vu et al.).
Liknande uppdatering för COVID-19-vaccin och influensavaccin
Principen hur de uppdaterade bivalenta boostervaccinen tas fram och börjar användas, påminner en del om hur man gör för influensavaccinen: Vaccinen kan med årlig basis uppdateras utifrån de stammar av influensavirus som man tror kommer att cirkulera, mot hösten och vintern av den kommande influensasäsongen. Preklinisk data har funnits en längre tid för de mer uppdaterade bivalenta vaccinen, och har t.ex. redovisats för amerikanska CDC.
Eftersom BA.4/5 nu dominerar i flera delar av världen (t.ex. i USA), så har många argumenterat för att det är mot de nu dominanta Omicron-varianterna som vi bör försöka vaccinera oss mot. Därtill argumenterar många att förändringen i vaccinen är relativt liten: Det rör sig om ett antal förändringar i mRNA-sekvensen (mot Spike-proteinet som vi immuniserar mot). Detta kan sägas vara betydligt mindre omfattande ändringar än de som vi ibland behöver göra för influensavaccinet, eftersom influensavirus i stället kan ha helt olika gensegment från säsong till säsong.
För övrigt så använder vi nuförtiden vaccin riktade mot upp till fyra influensavirus (tetravalenta vaccin). Därmed liknar de nyare bivalenta COVID-19-vaccin i viss mån våra influensavaccin.
Behövs en fjärde dos?
Vissa har däremot ifrågasatt huruvida de uppdaterade vaccinen verkligen behövs, delvis mot bakgrunden att vi redan har välfungerande vaccin mot COVID-19 (om man avser det ursprungliga målet att skydda mot svår sjukdom i COVID-19). Därtill kan större delen av skyddet som även uppdaterade vaccin ger mot infektion eventuellt vara ganska övergående (då den delvis beror på höga nivåer av neutraliserande antikroppar, som immuncellerna naturligt låter sjunka med tiden).
Skyddet mot allvarlig COVID-19 (t.ex. från CDC) tycks därtill enligt en hel del data — men inte all — bestå ganska väl över tid, åtminstone före Omicrons intåg. Hur bestående skyddet mot svår COVID-19 är under Omicron-perioden tycks ännu vara mer okänt. Därtill är det ännu relativt okänt hur väl vaccinen skyddar mot långtidscovid, särskilt under Omicron-dominanta perioder. Detta mot en bakgrund att en hel del fortfarande rapporterar rätt långvariga besvär efter en SARS-CoV-2-infektion: Enligt en nyare preprintstudie hade runt en femtedel (21%) under sommarperioden besvär som kvarstod åtminstone i fyra veckors tid.
Viss data tyder på att vaccinen avsevärt minskar risken för långtidscovid, även nu under Omicron-dominanta perioder. Annan data pekar på att riskminskningen är betydligt mindre påtaglig: Estimaten varierar med 15-80% riskminskning, enligt en nyare sammanställning. Skillnader kan ha att göra med vilka åldersgrupper som studeras, samt vilka varianter som man smittas av.
I detta sammanhang är det kanske värt att nämna, att många inte heller trodde att en 3:e vaccindos (en första boosterdos) skulle behövas — inte ens efter att Omicron tillkom. Nu anser dock många, däribland just tidigare kritiker mot en 3:e dos, att vaccinen bör anses utgöras av åtminstone en tredosserie.
Samtidigt argumenterar alltså många för att man bör ta en 4:e dos. Detta utifrån att Omicron är en så pass annorlunda variant. Därtill tycks som tidigare nämnt boosters riktade mot Omicron kunna förbättra skyddet både mot olika Omicron-varianter, liksom mot andra mer annorlunda (och därmed ev. framtida) varianter.
I sammanhanget hänvisas också till faktumet att de långsiktiga riskerna med SARS-CoV-2-infektioner ännu är dåligt kartlagda. Här kan man jämföra med multipel skleros (MS), där man nyligen funnit att tidigare infektion med det vanliga Epstein-Barr-viruset (EBV, som orsakar mononukleos, körtelfeber) tycks vara en mycket kraftig prospektiv riskfaktor för MS. Osäkerheten gällande COVID-19 gäller eventuellt även för riskerna som upprepade infektioner kan innebära, där vi ännu enbart har ofullständig data för eventuella långtidsrisker.
T.ex. finns data som tyder på att även mild COVID-19 (åtminstone hos mestadels ovaccinerade) exempelvis kan öka risken för negativa effekter på hjärnans struktur, utöver de besvär som många kan få vid långtidscovid (såsom lukt- och smakbortfall). En nyare sammanställning tyder t.ex. på att runt 30% av de med luktstörningar kan ha kvarstående subjektiva besvär runt två år senare.
Skyddet mot COVID-19 från en fjärde dos av originalvaccinen
En fjärde vaccindos (2:a booster) tycks åtminstone i några månaders tid öka skyddet mot alla former av COVID-19. Men den mest påtagliga – och kanske enda bestående – ökningen är för skyddet mot svår COVID-19. Ju längre tid som gått sen dos 3, desto bättre tycktes ökningen av skyddet mot dödlig COVID-19, i en svensk studie av Nordström et al. med data från äldreboenden. Dos 3-4 tycks genomgående öka skyddet mot svår COVID-19, även om de flesta studier har gjorts bland äldre individer.
Många av följande studier utfördes därtill under perioder där tidigare Omicron-subvarianter dominerade. Skyddseffekten mot svår COVID-19 tycks dock även öka relativt påtagligt mot de nyare varianterna BA.4/5, om man har tagit en 3:e eller 4:e dos av våra ursprungliga mRNA-vaccin mot COVID-19. Detta enligt ny preliminär studiedata, samt CDC-datan som listas längre ner. BA.4/5-subvarianterna utgör >85% av alla COVID-19-fall i t.ex. USA.
- Tilläggs-skyddseffekten för en 4:e jämfört med 3:e vaccindos, var i en israelisk studie ~64% mot allvarlig COVID-19, samt 76% mot COVID-19-relaterade dödsfall.
- I en annan studie sågs på några veckors sikt runt 3,5-4 gånger lägre risk för svår COVID-19, hos dem som hade fått fyra jämfört med tre doser av Pfizer-BioNTechs mRNA-vaccin. Det ytterligare skyddet som den 4:e dosen gav mot allvarlig COVID-19 tycktes också hålla väl över den (begränsade) tid som studien omfattade.
- En CDC-studie studerade effekten på COVID-19-associerad sjukhusvistelse: Skyddet ökade från cirka 55 % vid ≥120 dagar efter den 3:e dosen, till cirka 80 % efter den 4:e dosen.
- I studier i the Lancet och BMJ, studerades äldre individer. I den ena studien – Lancet-studien från Sverige – sågs att för de som var 80+, så gav den 4:e dosen ungefär 54-71 % ökat skydd jämfört med den 3:e dosen.
- CDC redovisar löpande data för hur vaccinens skydd mot COVID-19 håller: Ett tydligt ökat skydd ses även där vad gäller mot dödlig COVID-19, för den 4:e jämfört med 3:e dosen — med en riskhalvering. Att detta håller ända in i slutet av juli, tyder sannolikt på att det ökade skyddet även håller mot de nu dominanta Omicron-subvarianterna.
Hybrid immunitet: Skyddet som vaccin kombinerat med en Omicron-infektion kan ge
I en ny NEJM-studie har man även bedömt att en genombrottsinfektion (dvs. infektion hos tidigare vaccinerade) med varianterna BA.1/2, vilka cirkulerade i vintras till våras, ger ett hyfsat bra skydd mot infektion med de senare varianterna BA.4/5 — upp mot 75% skydd. Skyddet mot BA.4/5 var betydligt lägre hos de som hade fått en infektion med en tidigare variant (före Omicron tog över, såsom med Deltavarianten).
Denna analys har gjorts utifrån omfattande nationell portugisisk data och redovisas i tidskriften NEJM. Detta gäller dock mot en bakgrund av mycket hög vaccinationstäckning i Portugal: I studiepopulationen var närmast alla (98%) fulldosvaccinerade innan år 2022.
Tidigare och nyare data tyder nämligen på att en infektion med Omicron i sig – dvs. utan kombinationen av annat immunologiskt skydd (t.ex. från vaccin) – ger dålig immunitet mot andra varianter. Detta finns det nu även data som pekar på samma bristfälliga infektionsmedierade skydd från Omicron även ses hos barn (åtmintsone utifrån antikroppsnivåer).
Däremot tyder samma preprintstudie på att barn som hade vaccinerats, fick ett mycket bättre skydd mot Omicronvarianter. Detta stämmer även överens med data publicerad i NEJM, där man såg att skyddet mot reinfektion var betydligt högre hos vaccinerade barn som fick en genombrottsinfektion (~79% jämfört med ~63% hos ovaccinerade barn).
Detta kan vara värt att beakta utifrån huruvida länder och olika individer har valt eller inte valt att vaccinera sina barn, med avseende på risken för reinfektion och de eventuella långvariga besvär (långtidscovid) och andra tillstånd (t.ex. MIS-C) som det kan innebära.
Below: Screenshot of Figure S4 from Chalkias et al. (N Engl J Med. 2022). Shows that the BA.1-directed bivalent booster from Moderna (mRNA-1273.214) elicits higher neutralizing antibody levels against BA.4/5 subvariants, compared with the original (monovalent) Moderna vaccine, mRNA-1273. Note that the y scale shows logarithmic values.