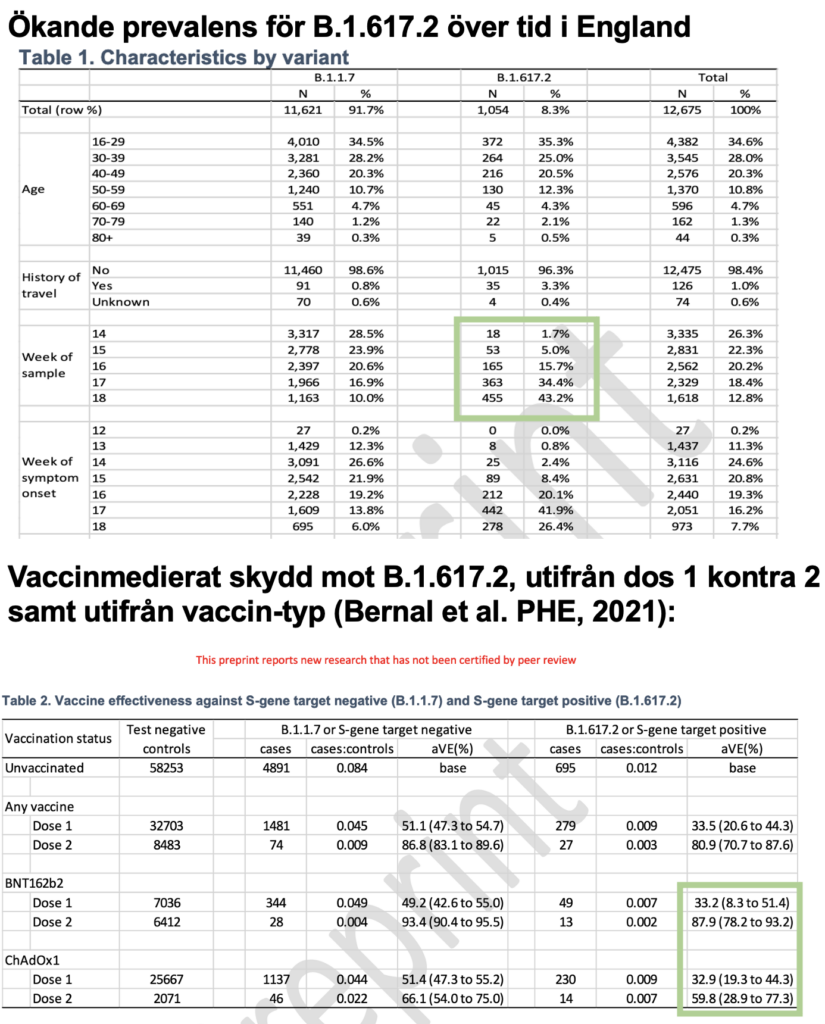
I dagarna har vad som tycks vara den första immunologiska datan för heterolog prime boosting kommit: Spansk data från studien CombivacS, med några hundra deltagare, visar att en dos av AstraZenecas vaccin, följt av en dos av Pfizers vaccin, ger en mycket påtaglig stegring av neutraliserande antikroppar – en ökning med faktor 42-150, beroende på undersökt antigen. Än saknas dock så kallad effectiveness-data för denna typ av kombination. En längre beskrivning följer nedan.
Denna studie heter CombivacS (dvs. ej samma som engelska studierna COM-COV1/2), och omfattar deltagare som är yngre än 60 år gamla. Det är en randomiserad fas 2-studie där fem spanska sjukhus ingår. Deltagarna tycks i sin helhet komma att följas i över ett år.
- De rekryterade 663 deltagare som fått en första dos AstraZeneca. Två tredjedelar slumpades till att få Pfizers vaccin, 8 veckor efter den första dosen. En kontrollgrupp fick inget vaccin som booster (dvs. avvaktade).
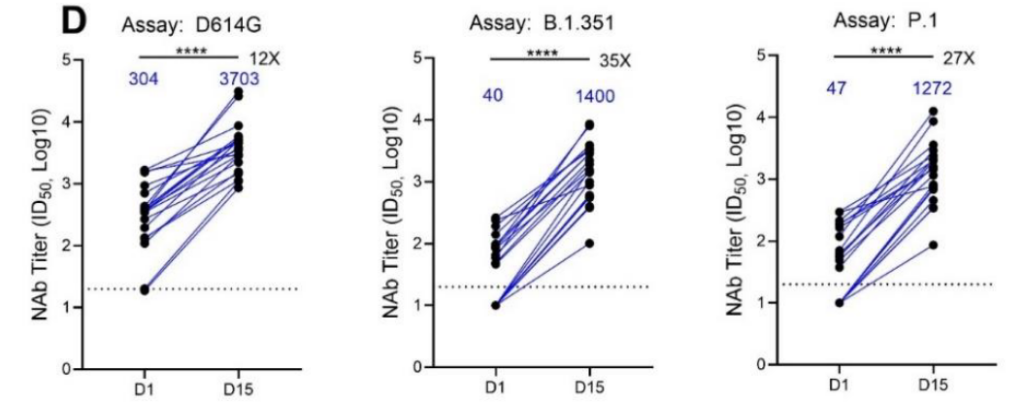
- Forskarna fann att kontrolldeltagarna inte uppvisade förändringar över tid i deras antikroppar, uppvisade de som fått Pfizers vaccin som andrados 123 till 150 gånger högre nivåer av antikroppar (räknat 7 respektive 14 dagar efter boosterdosen). Antikropparna mot receptorbindande domänen (RbD) ökade alltså från 58 till 9102. Mot hela trimeriska spike-proteinet ökade nivåerna från 82 till 3430 enheter – faktor ~42.
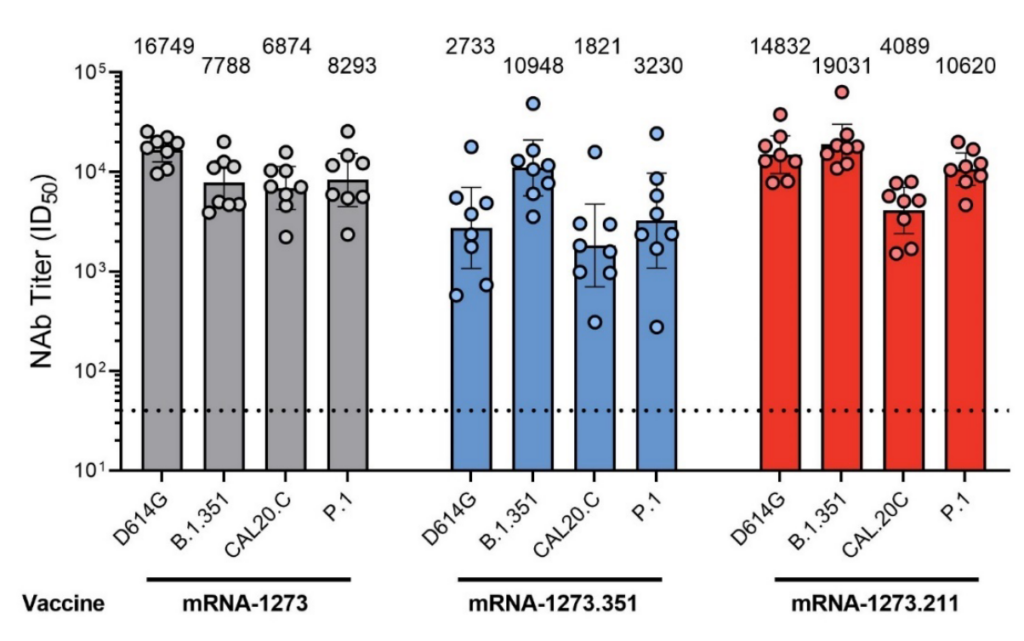
- Kombinationen av olika vaccin gav också sju gånger högre neutralisering mot SARS-CoV-2, att jämföra med 3 gånger högre neutralisering som setts tidigare efter andra dosen av AstraZenecas vaccin.
- De ska även ha följt biverkningar (se även nedan) som inte tytt på att några har fått reaktioner som krävt medicinsk undersökning eller sjukhusvård. T.ex. var huvudvärk (44%), obehag (41%), frossa (25%), milt illamående (11%) och feber (2.5%) vanligt.
- Datan ska ha undersökts av en oberoende data safety monitoring board, dvs. ett standardiserat säkerhetsförfarande för bland annat läkemedelsstudier, där man kan tänka sig att en eventuell risk för deltagare kan föreligga och därför av säkerhetsskäl bör bevaka studiedatan noggrant under studiens gång.
- Nyligen kom också tidig data från studien COM-COV – samt en tysk pågående studie – som båda indikerar att säkerheten tycks god när man kombinerar AstraZeneca och Pfizer i någon ordning för dos 1 och 2, utifrån data i bland annat The Lancet Infectious Diseases. Här väntas dock immunologisk data först i juni.
- Lite kopplat till denna studie, har en preprintstudie om biverkningar kommit för SputnikV (som faktiskt är ett heterologt prime-boost-vaccin, då man har olika serotyper av adenovirus för prime och boosterdosen). De observerade att de som hade någon typ av biverkningar vid den andra dosen, hade högre sannolikhet för att uppleva biverkningar efter den första dosen (givetvis självrapporterat, så det kan finnas bias – men kan vara intressant för att förstå interindividuella skillnader i risken för biverkningar).
Dessvärre är ovanstående resultat från studien CombivacS bara presenterat online på spanska den 18:e maj. De flesta av resultaten är tagna från den presentationen (då preprint-data saknas). Därtill saknas ju viktiga kontrollgrupper (dvs. de som fått två doser av AstraZenecas vaccin eller först Pfizer och sen AstraZenecas vaccin).
Med vänliga hälsningar,
Jonathan Cedernaes
Leg. läkare, PhD/senior forskare