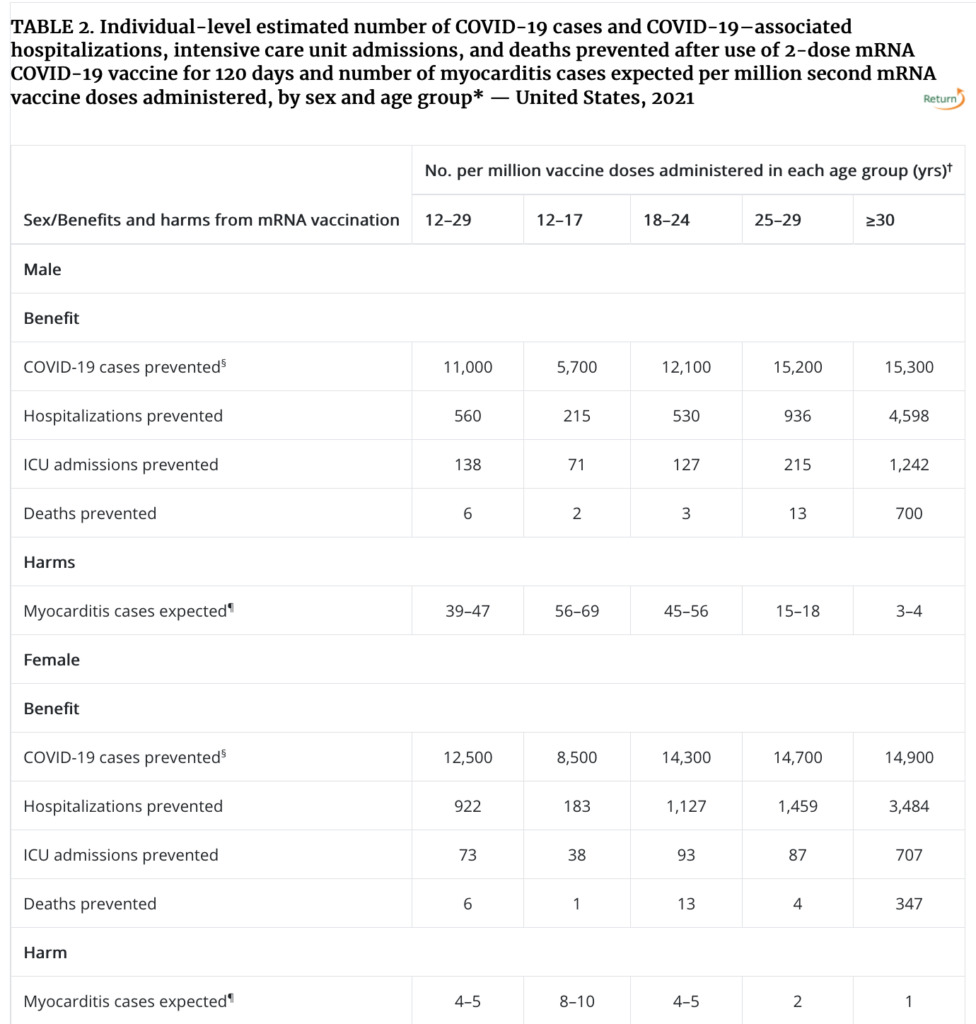
- De med tidigare COVID-19 hade enligt en av analyserna ett hyfsat skydd mot infektion med Omicron (som dock var betydligt lägre enligt en annan analys, se nedan samt punkt 2), men skyddet var i den nya analysen deskriptivt lägre än för de som hade fått tre doser vaccin.
- Som redogörs här i inlägget är emellertid det viktiga skyddet mot svår COVID-19 orsakad av Omikron mycket robustare över tid, jämfört med skyddet mot infektion i sig. Detta har man i senare data visat sig håller väl över tid (≥3 månader) på en hög nivå efter tre doser (~90% riskreduktion), jämfört med en lägre skyddseffekt efter enbart två doser (~50-70% skydd)..
- Enligt ny brittisk preliminär data redovisad nedan så ses sådant gott skydd mot svår COVID-19 orsakad av Omicron-varianten även för den äldre gruppen (65+), för de som har fått 3 doser vaccin. Att skyddet är avsevärt högre för gruppen som fått tre kontra två vaccindoser, stöds även av en sydafrikansk studie i New England Journal of Medicine (två doser gav ~70% skydd), samt ytterligare preliminär brittisk data: I en bredare åldersgrupp ökade skyddet från 44-68% med två doser, till 83-92% efter tre doser (i annan data från ~70% till ~90%).
- För gruppen 65+, var emellertid skyddet som 3 doser gav mot symptomatisk COVID-19 orsakad av Omicron, betydligt lägre än skyddet mot svår COVID-19: Runt 50% skydd sågs vecka 5-9 efter 3:e dosen (därefter ev. ner mot 30% vid perioden ≥10 veckor). Därtill ses kanske åtminstone en indikation, liksom i viss tidigare data, för att skyddet kan vara något högre på sikt för de som fått Moderna som booster (tidigare tvådosdata som indikerar detta har observerats i jämförelser av Moderna kontra Pfizer; se även denna meta-analys).
I en annan analys från Skottland (se skärmdump här nedanför, samt punkt 2) undersöktes alltså vaccinskyddet mot infektion i sig med Omicron-varianten, för gruppen 18 år och uppåt. Här ser vi att efter enbart 2 doser tycks skyddet mot infektion i sig med Omicron-varianten vara helt borta på sikt, hos gruppen 18+. Observera att detta alltså ej är detsamma som skyddet mot svår COVID-19 – det är generellt sett betydligt svårare att erhålla skydd mot infektion än mot symptomatisk eller svår COVID-19 (för detta tycks i fallet SARS-CoV-2 krävas höga nivåer av neutraliserande antikroppar, och det är naturligt att nivån av dessa avtar över tid).
- Efter en (3:e) boosterdos, återställdes dock – åtminstone tillfälligt – i hög grad skyddet mot infektion i sig med Omicron (~68-71% skydd; ~59-65% efter justering för tidseffekt, så kallad “waning”). Individerna tycks ha fått den 3:e dosen runt 7 veckor tidigare (detta avser vuxna i åldern 18+, och utgör också preliminär brittisk data). Utifrån den tidsdynamik som ses i många av dessa analyser kan man dock anta att detta skydd också avtar mer över tid (liksom meta-analysen tyder på, utifrån data som inkluderade skyddet mot Delta-varianten).
- Efter 3 doser finns det nu även preliminär data som tyder på att nivåerna av antikroppar (specifika mot
Omicron-varianten) ligger kvar på en skyddande nivå i åtminstone upp till 3 månader (antikroppar utgör en del av immunförsvaret, höga nivåer kan hjälpa ytterligare för skyddet mot infektion och symptomatisk COVID-19). - Notera också att dessa analyser finner att skyddet mot infektion med Delta-varianten var ganska välbevarat över tid efter “enbart” 2 doser vaccin: runt 70% skydd efter två doser (med en andrados given runt 5 månader tidigare). Dock var detta ej någon slumpmässig provtagning, så sannolikt föreligger bias mot symptomatiska infektioner. Annan data finner samtidigt att skyddet mot svår sjukdom med Deltavarianten har varit extremt välbevarat över tid, särskilt hos yngre, även efter två vaccindoser. Men observera att vaccinen alltså skyddar sämre mot Omicron, särskilt efter enbart två vaccindoser, och särskilt mot infektion i sig – skyddet mot svår sjukdom är alltså enligt ovan betydligt mer välbevarat efter tre doser.
- Medan skyddet mot infektion i sig med Omicron-varianten därmed är mycket lågt, har tidigare data har samtidigt visat på ett hyfsat skydd mot symptomatisk COVID-19 orsakad av Omicron-varianten, i åtminstone någon månad efter 2 doser av mRNA-vaccin (men ej efter enbart 2 doser av AstraZenecas vaccin, se preprint-studien av Andrews et al.; Twitter-tråd här, samt en längre Facebook-sammanfattning här). Detta skydd tycktes dock i enlighet med ovanstående analyser vara betydligt bättre efter tre vaccindoser.
- Den nya Skotska preprint-analysen fann också att skyddet mot infektion i sig (att testa positivt) med Omicron-varianten var ganska bevarat efter tidigare COVID-19 (enbart tidigare infektion, dvs. ej vaccinerade individer). Skyddet var runt 53%, men det var ändå betydligt lägre än vad tidigare COVID-19 gav mot Delta (runt 89% skydd). Detta skiljer sig från Imperials beräkning på skydd mot Omicron-infektion i sig på ~19% efter tidigare COVID-19, så här kan det ännu finnas en osäkerhet eller variation utifrån exempelvis studerad population eller tid efter en föregående infektion.
På slutet redogör jag i en separat punkt just för studier som visar att vaccinen har fungerat väl även över tid mot tidigare varianter, dvs. inklusive för Delta-varianten (punkt 3). Detta avser framförallt skyddet mot svår och dödlig COVID-19, och stöds av meta-analysdata som finner att vaccineffekten för detta skydd avtog sparsamt över sex månaders tid (men detta gäller återigen Delta-varianten; vi saknar ännu motsvarande data för hur vaccinskyddet på sikt ter sig mot Omicron-varianten).
1. Very good protection against severe COVID-19 caused by Omicron, even among those aged 65+, who have received 3 vaccine doses
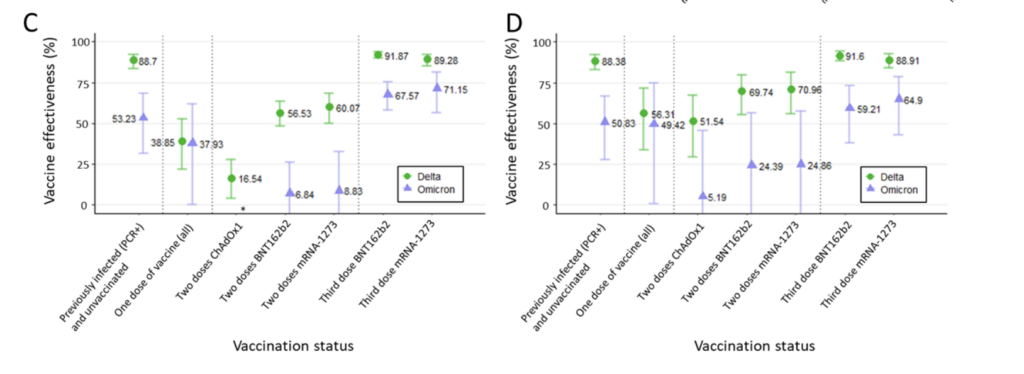
- 89% at 10 weeks and onward (may drop somewhat later).
- The protection was 94% up until and including week 9 (please see the screenshot below).
- In analyses of the symptomatic cases (meaning, how likely is a symptomatic case to get hospitalized) protection was around this range (85-89%) in this older, more vulnerable age group.
(second link if the above one doesn’t work)
- The above data can also be complemented data from South Africa, where a study at NEJM, by Collie et al., found ~70% protection against hospitalization due to COVID-19 after just two doses. Remember that South Africa has a relatively young population – here, most (24.2%) admissions were in the 30-39 age group – so this may not be representative for a broader population.
- Related to the broader age group in the U.K., a preliminary report (the Jan 14 Technical briefing #34), found that vaccine-mediated protection against the risk of hospitalization (from COVID-19 with Omicron), was initially over 90% from three doses, and declined somewhat to ~83% after 10+ weeks. However, the corresponding protection after only 2 doses was considerably lower (initially 58-64%, but at 44% at the 6-month time point)
- In the 65+ age group, protection was minimal or absent against mild symptomatic omicron COVID-19 when examining the period 20 weeks after receipt of only 2 vaccine doses (Pfizer or Astrazeneca vaccine recipients).
- However, after a third (booster) dose, effectiveness rose to 62-65% at week 2-4 in those who had initially received AstraZeneca‘s vaccine, but was down to 48-56% at week 5-9 .
- Those aged 65+ who had been vaccinated with 3 doses of Pfizer’s vaccine had 65% protection from mild omicron COVID-19 at week 2-4, but this was down to 49% at week 5-9, and only at 31% starting at week 10.
- Those vaccinated with 2 doses of Pfizer’s vaccine followed by a Moderna booster, had 70% protection from mild omicron COVID-19 at 2-4 weeks after the booster; down to to 57% at 5-9 weeks.
Below is a screenshot of Table 1 from the Jan 7 (2022) analysis from the UK Health Security Agency – this applies to the age group 65+, but as detailed above, the data seems similar for based on a broader age group.
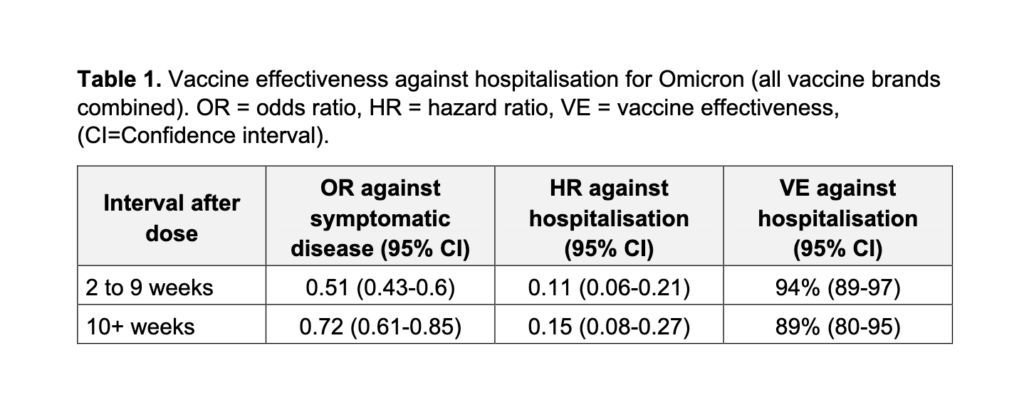
2. A third (booster) dose with the mRNA vaccines significantly increased protection against infection & symptomatic COVID-19 caused by Omicron
- After a period about 5 months after just 2 doses, protection against infection with the Omicron variant was basically gone (see figure). But note, this refers to protection against infection itself – vaccine-mediated protection against severe COVID-19 is much higher (as detailed in summary 1 above).
- Protection was however maintained at ~52% in those with prior COVID-19. This is far higher than the 19% protection against infection with Omicron from prior COVID-19, that was calculated by Imperial College London researchers, so there may still be some uncertainties in the exact protection afforded from just prior COVID-19, against infection with the Omicron variant. At the same time, preprint data based on in vitro studies (see also this preprint data) suggest that those with prior COVID-19 who get vaccinated, will achieve similar protection against Omicron, as those who have received three vaccine doses.
- However, after a third (booster) dose, with Pfizer or Moderna’s vaccine, protection rose to ~68% and 71% against Omicron, respectively, and was thus at a higher level than after prior COVID-19 (likely, those with prior COVID-19 would achieve similar or higher protection if they got vaccinated).
- When waning was taken into account, these figures were slightly lower, at ~59% and 65%, respectively, after booster doses with Pfizer’s and Moderna’s mRNA vaccines.
- Overall, this data is thus consistent with prior preprint data by Andrews et al., which I have described previously on Twitter, and Facebook. The data is also somewhat consistent with a new preprint by Buchan et al. and by Tseng et al., who examined the effectiveness from a Moderna booster (3rd dose) against Omicron (these latter studies are described in the next section).
- This data is also consistent with the preliminary Jan 14 Technical briefing (#34) from the UKHSA, which however found that protection, after 3 vaccine doses, against symptomatic COVID-19 due to Omicron dropped to 45-50% at week 10 and onwards. While there wasn’t enough data for the Moderna booster, protection may have held better over time (i.e., at 10+ weeks) – this may be revealed by later data.
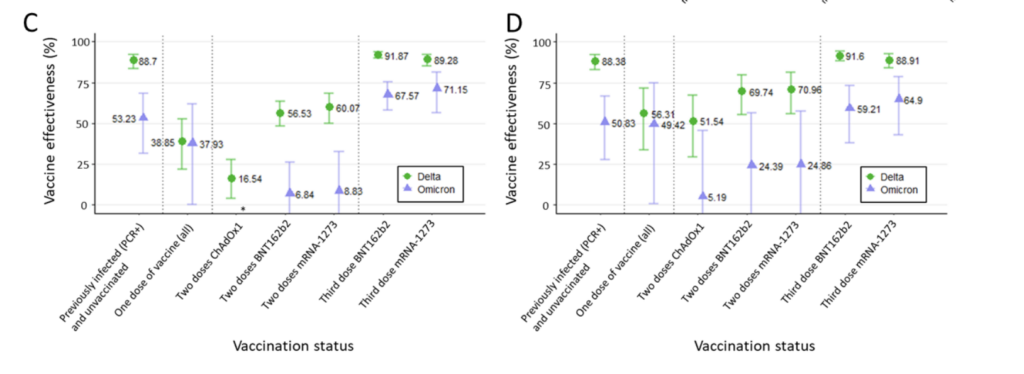
Buchan et al.: Around 37% protection against infection with the Omicron variant ≥7 days after receiving a mRNA vaccine as the 3rd dose – but no protection against infection itself, after only 2 doses. This was based on 3,442 Omicron-positive cases, 9,201 Delta-positive cases, and 471,545 test-negative controls.
Tseng et al.: Recipients of 3 doses of Moderna’s mRNA vaccine had an initial vaccine effectiveness around 95% (93%-96%) against infection with the delta variant, but a lower 62.5% (56%-68%) against infection with the Omicron variant, in those who were recently (~5 weeks earlier) vaccinated. In those who received their third dose around 15 weeks earlier, effectiveness was ~49%.
- This analysis was based on 6657 cases that tested positive (56% omicron; 44% delta), and the numbers above apply to the immunocompetent individuals (meaning they had intact immune systems).
- They also saw that 2-dose recipients of Moderna’s vaccine, initially had some protection against infection with the Omicron variant (~30% day 14-90), but this was gone at later time points.
- Here they also studied the 3-dose vaccine effectiveness against infection with the Omicron variant in immunocompromised individuals, and found quite low protection (11.5%; 95% CI 0%-67%).
Andrews et al.: Here 3 vaccine doses provided around 70-75% protection against symptomatic COVID-19 caused by the Omicron variant, in an analysis based on 56,439 Delta and 581 Omicron cases, and 130,867 test-negative controls.
- This was calculated at the point of 2 weeks or longer after a third (booster) dose with Pfizer’s mRNA vaccine, with:
- ~71% protection among those who received AstraZeneca as the primary vaccine course (2 doses), followed by a Pfizer dose (a total of 3 doses).
- ~76% protection among those who received 3 doses of Pfizer’s vaccine (see screenshot below).
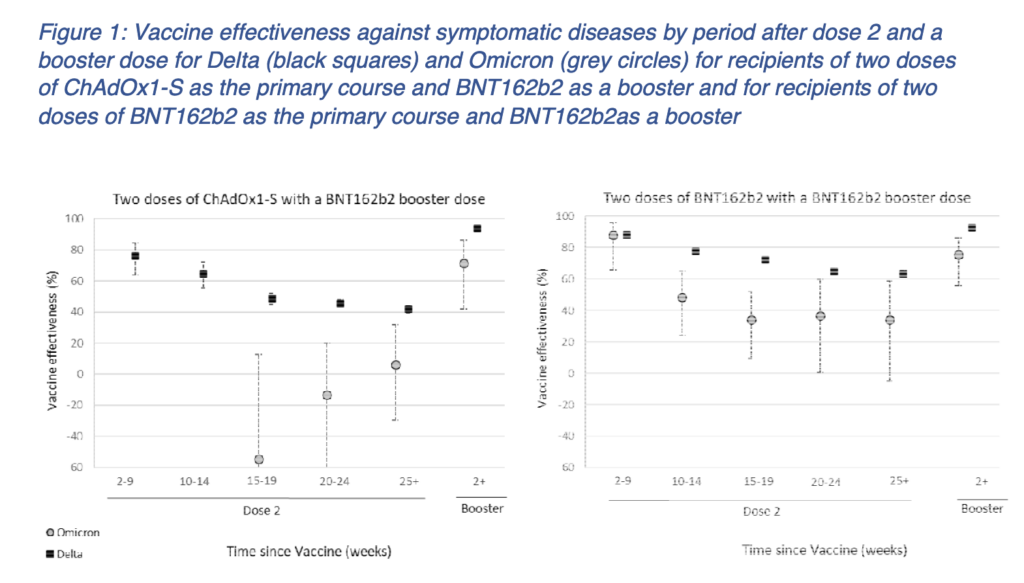
- Here they also noted that 2 doses of Pfizer’s mRNA vaccine may at least initially offer some protection against symptomatic COVID-19 caused by the Omicron variant (at 88% at week 2-9 after the second dose; ~48.5% at week 10-14, and ~34-37% at 15+ weeks).
- This effect was thus overall a) at an overall lower level than after a booster, and b) this effect seems to be very low (wide interval) starting already at week 15, being gone after around 5 months. But again, please note that this specific analysis only applies to protection against symptomatic, not severe, COVID-19, and specifically that caused by the Omicron variant.
- Note that this analysis was based on quite early data and did not include that many Omicron cases. Furthermore, the observation that the estimates are negative at earlier weeks post dose 2 for AstraZeneca, is likely explained by this group including older individuals with more co-morbidities.
- Against the Delta variant: This analysis also indicates that even after 6 months (see Figure 1), protection was still >60% against symptomatic COVID-19 caused by the Delta variant, in those who had received just 2 Pfizer mRNA vaccine doses (so as expected based on the other data presented above, higher than against the Omicron variant). Similar findings were seen above in the Tseng et al. preprint (see also the next summary regarding vaccine-mediated protection against the Delta variant)
Similar data was more recently reported in the 34th technical briefing from UKHSA:
- For those who had received 2 doses of either the Pfizer or Moderna mRNA vaccines, around 20 weeks after the 2nd dose, effectiveness had dropped (from ~65-70%) to ~10%.
- At ~2-4 weeks after the 3rd dose (a booster), protection against symptomatic COVID-19 caused by Omicon was ~65-75%. However, this dropped to ~55-65% at the 5-9-week period, and to ~45-50% at and beyond 10 weeks after receiving this 3rd vaccine dose.
- At 3 months time after receiving the 3rd vaccine dose, there is now also preliminary data showing that antibody levels remain at a level that can neutralize the Omicron variant to some extent.
Below is a screenshot from Figure 1 from Andrews et al. (described above)
3. During the Delta period vaccines continued to provide good protection against infections and hospitalization – especially with an added third vaccine dose
After six months, a second mRNA vaccine dose offered ~45% protection for Pfizer recipients, and ~65% for Moderna vaccine recipients, against infection with SARS-CoV-2, during a period when the Delta variant dominated.
With a third (booster) mRNA vaccine dose, these figures rose to ~88% and 91%, respectively.
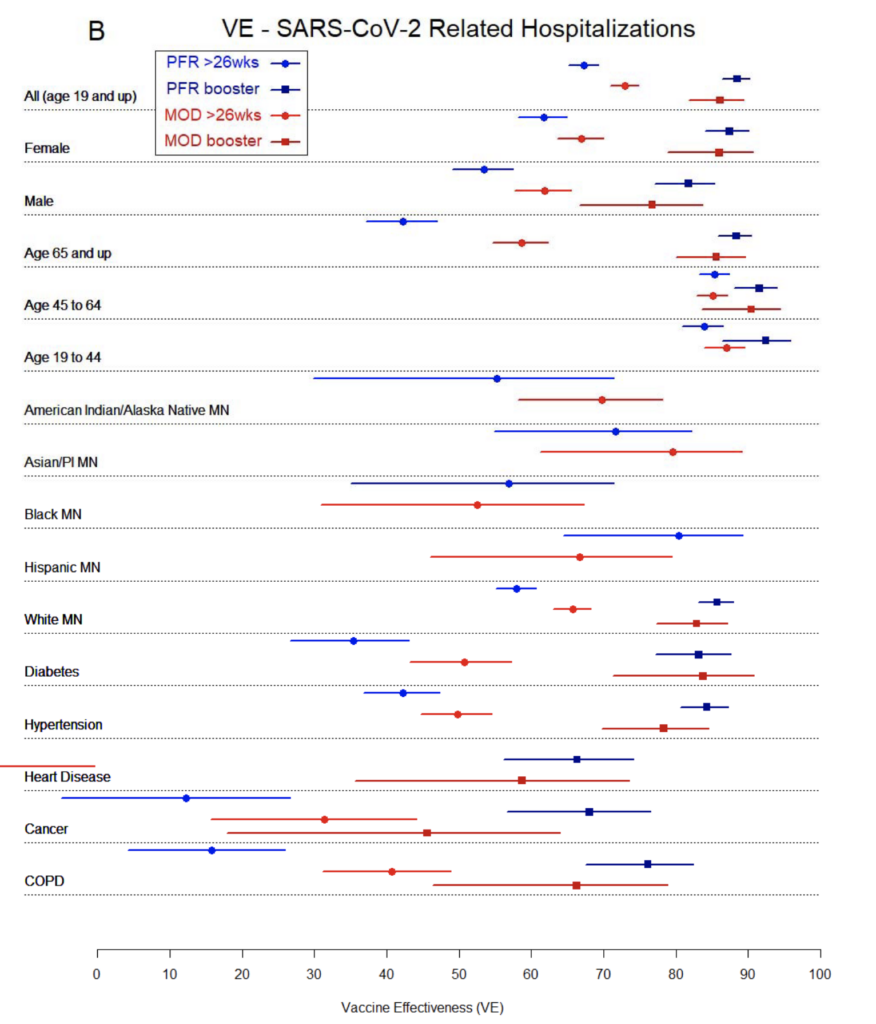
Against hospitalization, six months after a second dose, vaccine effectiveness against COVID-19 hospitalizations, was ~67% for Pfizer recipients and ~73% for Moderna vaccine recipients. These figures rose to 88% and 86%, respectively, in participants who had received a third (booster) dose.
What this data also shows, is that in the 19-64 age groups, even at the 6-month time point and from just two mRNA vaccine doses, protection was very good against severe COVID-19 caused by the Delta variant.
However, at the same time, the data shows that in individuals who had a range of co-morbidities (that are known to increase the risk of severe COVID-19), protection was quite low against hospitalization with the Delta variant, from just two mRNA vaccine doses. However, almost across the board, that protection increased significantly in those who had received a third (booster) dose of the mRNA vaccines.
That protection against hospitalization is maintained well over time, even against the Delta variant of SARS-CoV-2, is also supported by a November 2021 preprint meta analysis, by Feikin et al..
- In that preprint, they found a decline in vaccine effectiveness over time (they used or inferred six-month data). However, this decline was most notable for vaccine-mediated protection against infection & symptomatic disease, in the ~20-32% range.
- Against any type of SARS-CoV-2 infection (i.e. including asymptomatic infection), vaccine effectiveness dropped ~19-20%. This was consistent across all ages, when examining a mix of variants (but of course this did not include assessments for protection against Omicron, as this analysis was posted in November, 2021).
- The decline over time was far less pronounced against severe COVID-19, as vaccine effectiveness was maintained at >70% in all the included studies. Against severe COVID-19, no study showed a ≥25% drop in vaccine effectiveness over the 6-month analysis period. Overall, for this outcome over time, the drop in vaccine effectiveness was ~8% for all ages; and ~9.7% for older individuals.
An example of a (preprint) study that was included in the above meta analysis, and which showed high vaccine-mediated protection over time against hospitalization and death, is the 2021 preprint by Lin et al., which has since been published in the New England Journal of Medicine. This is based on data from ~10.6 million North Carolina residents. That study found that at 7 months after the second dose, vaccine-mediated protection was >80% against symptomatic infection for Moderna mRNA vaccine recipients, and ~67% for Pfizer vaccine recipients (again, this does not cover Omicron). At this 7-month time point, protection was at an even higher 89-94% against severe COVID-19, and 90.5-95.5% protective against death due to COVID-19, among recipients of the Moderna and Pfizer mRNA vaccines.
Below: a screenshot from the preprint by Drawz et al., showing vaccine-mediated protection from Pfizer’s vaccine (PFR) and Moderna’s vaccine (MOD), at a period when the Delta variant was dominant. Protection estimated for the period >6 months (“>26wks”) after 2 doses, and with a third (“booster”) dose.